Vediamo ora alcuni esperimenti di laboratorio.
Gli apparecchi usati sono quelli rappresentati nella figura e negli schemi.
II primo esperimento mostra dome si sintetizza l'acetofenone, un composto che si usa per preparare un'ampia serie di altri composti organici. Nel compierlo dobbiamo ricordare due cose:
1. molte reazioni chimiche necessitano di calore;
2. troppo calore puņ decomporre alcuni composti organici.
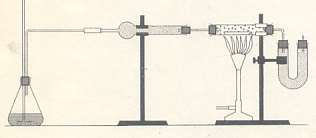
Ecco come un chimico descriverebbe l'esperimento: si introduce l'anidride acetica nella parte superiore dell'apparecchio per mezzo di un imbuto a goccia; essa raggiunge, attraverso il tubo interno, il palloncino che contiene benzolo e cloruro di alluminio. Poiché abbiamo bisogno di una temperatura costante, il palloncino č immerso in un bagno d'acqua riscaldata continuamente da una fiamma. In questo esperimento l'anidride acetica evapora facilmente e quindi abbiamo attaccato al palloncino un condensatore (Liebig), il quale consiste di un tubo inserito all'interno di un altro, di dimensioni maggiori, in cui vien fatta circolare acqua fredda. La maggior parte del vapore si ritrasforma cosķ in liquido e ritorna al palloncino; il vapore che supera il condensatore entra nel lungo tubo di vetro (a destra nella figura) e scende in un recipiente, dove viene assorbito da idrossido di sodio.
Reazioni simili a quella che abbiamo ora descritto servono a sintetizzare molti composti organici e hanno consentito ai chimici di creare utili composti che non si trovano in natura.
II nostro secondo esperimento dimostra come calcolare i pesi di combinazione dell'idrogeno e dell'ossigeno. I chimici hanno potuto determinare i pesi relativi dei diversi elementi e costruire cosģ un sistema relativo di pesi atomici, proprio in seguito a tutta una serie di esperimenti sui pesi di combinazione (oltre ad esperimenti di altro genere).
Per ottenere idrogeno mettiamo dello zinco in un matraccio e aggiungiamo acido solforico; l'idrogeno č quindi essiccato in un tubo contenente cloruro di calcio che assorbe il vapore acqueo. L'idrogeno secco passa in un tubo in cui si trova una vaschetta di porcellana contenente ossido di rame riscaldato. L'idrogeno separa l'ossigeno dall'ossido di rame, lasciando solo il rame. Il vapore acqueo prodotto dalla combinazione dell'idrogeno con l'ossigeno č assorbito dal cloruro di calcio contenuto nel tubo a U.
Se pesiamo l'ossido di rame prima dell'esperimento e il rame dopo l'esperimento, la perdita di peso ci dice la quantitą di ossigeno allontanata dall'idrogeno. Anche il tubo a U contenente cloruro di calcio viene pesato prima e dopo l'esperimento: la differenza di peso constatata rappresenta il peso del vapore acqueo prodottosi per la combinazione dell'idrogeno con l'ossigeno dell'ossido di rame. Poiché conosciamo la quantitą d'ossigeno impiegata e la quantitą d'acqua formatasi, possiamo facilmente calcolare il peso dell'idrogeno usato. Conoscendo il peso dell'idrogeno e dell'ossigeno che hanno preso parte alla reazione possiamo anche calcolare il rapporto secondo il quale i due elementi si combinano. Nell'esempio citato risulta che otto parti in peso di ossigeno si combinano con una parte in peso di idrogeno.
|

Sopra: schema dell'apparecchiatura per la sintesi dell'acetofenone;
a sinistra il pallone e il bagno d'acqua, a destra il bicchiere con l'idrossido di sodio.
Sotto: apparecchiatura per determinare i pesi di combinazione dell'idrogeno e dell'ossigeno; a sinistra il matraccio con lo zinco, a destra il tubo a U.
|