Giuseppe Pignatale Presenta:

|
Fisica:
Il mondo dell'atomo:
RADIOATTIVITA' NATURALE.
Nella radioattivit‡ naturale alcuni elementi emettono particelle come protoni e neutroni giungendo dopo migliaia e migliaia di anni al piombo......
|
|
|
|
Sopra: a) un magnete deflette le particelle alfa, positive, e beta, negative, in direzioni opposte; i raggi gamma, neutri, non sono deviati. Gli elementi radioattivi possono produrre uno o pi˘ di questi tipi di raggi.
Sopra: b) un granello di radio, su una lastra fotografica emette particelle alfa; se ne possono osservare le tracce, 1/10 di mm al microscopio.
Sopra: c) una chiave posta fra un minerale radioattivo e una lastra fotografica avvolta in carta nera.;
Sopra: d) l'immagine della chiave ottenuta con lo sviluppo della lastra.
|
Spinti dalla scoperta dei coniugi Curie, gli scienziati scoprirono ben presto che tutti gli elementi con peso atomico superiore al bismuto
(vedi tavola periodica degli elementi) sono radioattivi: essi producono tre tipi di raggi, chiamati raggi alfa, beta e gamma. I raggi gamma sono onde elettromagnetiche come i raggi X, ma ancora pi˙ penetranti. I raggi beta sono come i raggi catodici, una corrente cioË di elettroni in rapido movimento, dotati di carica negativa. I raggi alfa sono una corrente di particelle pi˙ pesanti dei precedenti tipi di raggi - ognuna di esse pesa infatti circa quattro volte un atomo di idrogeno - e hanno una carica positiva uguale al doppio della carica di un elettrone. Questi tre tipi di raggi possono essere distinti l'uno dall'altro per mezzo di una calamita, che li deflette in tre direzioni diverse, vedi figura a sopra.
|
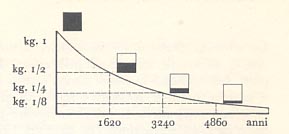
Periodo di semitrasformazione del radio: ogni
1620 anni la quantit‡ di radio si dimezza.
|
|
|
Lo studio di questi raggi, insieme a molte altre ricerche, conferma ciÚ che si Ë detto in precedenza: l'atomo Ë formato da un nucleo piccolissimo circondato
da un certo numero di elettroni in movimento lungo orbite ellittiche. Il nucleo possiede una carica elettrica positiva pari alla somma delle cariche negative degli elettroni, in modo che la carica totale dell'atomo sia zero. In un atomo, il numero degli elettroni nelle sue orbite o
il numero delle unit‡ di carica del nucleo si chiama numero atomico. Il peso di un atomo Ë praticamente uguale a quello del suo nucleo, perchÈ il peso degli elettroni Ë minimo.
Tutti gli atomi dello stesso elemento chimico hanno lo stesso numero di elettroni in orbita. Per esempio, ogni atomo di cloro ha nelle orbite 17 elettroni; quelli esterni determinano quali composti puÚ formare. Non tutti gli atomi di cloro, tuttavia, hanno esattamente lo stesso peso. Esistono due tipi principali di aiomi di cloro, i cui nuclei pesano rispettivamente 35 e 37 volte il peso dell'atono pi˙ semplice, quello di idrogeno. Questi tipi diversi di cloro vengono chiamati isotopi. Gli isotopi di qualsiasi elemento hanno lo stesso numero atomico e le stesse propriet‡ chimiche, ma peso atomico diverso. In natura gli isotopi di cloro si trovano mescolati con una proporzione di tre atomi di CI, peso atomico 35, per ogni atomo di Cl,peso atomico 37, cosÏ che il peso atomico medio del cloro allo stato naturale si aggira intorno a 35,5. Molti elementi naturali sono in realt‡ miscugli di isotopi diversi.
Il nucleo di un atomo di idrogeno Ë una particella unitaria che si chiama protone. Gli scienziati hanno scoperto anche un'altra particella, il neutrone, privo di carica elettrica, il cui peso Ë quasi uguale a quello di un protone.
Un isotopo di un elemento, per esempio il cloro cl, viene cosÏ rappresentato:
| peso atomico | 35 |
|---|
| numero atomico | 17 | | | Simbolo elemento |
|---|
Possiamo quindi affermare che il nucleo del cloro Cl. con peso atomico 35, Ë formato da 17 protoni, con le rispettive cariche positive, e dai 18 neutroni necessari a completare il peso totale (18+17=35). II nucleo del Cl, avente peso atomico 37, contiene 17 protoni e 20 neutroni. Una particella alfa contiene due protoni e due neutroni, ed Ë effettiv:amentc simile al nucleo di un atomo di elio.
Le radiazioni emesse da un atomo radioattivo provengono dal nucleo. Il nucleo di un atomo di radio contiene 88 protoni e 138 neutroni: il suo peso atomico Ë quindi 226 (= 88 + 138) e il suo numero atomico 88. Se esso emette una particella alfa, il nucleo rimarr‡ con 86 protoni e 136 neutroni; il suo peso atomico sar‡ allora 222 e il numero atomico 86. Questo atomo contiene ora soltanto 86 elettroni in orbita e perciÚ si tratta di un atomo diverso con differenti propriet‡ chimiche; si avr‡ quindi un altro elemento: il radon.
La met‡ di una determinata quantit‡ di radio dopo 1620 anni si muta in radon; dopo altri 1620 anni la restante mezza quantit‡ di radio si trasforma in un quarto di radon pi˙ un quarto di radio. Dopo ancora 1620 anni si ha solo un ottavo della quantit‡ iniziale di radio e il processo continua sempre in questa proporzione. Possiamo quindi affermare che 1620 anni sono il periodo di semitrasformazione del radio. LÏ vita media dei diversi elementi radioattivi varia da 900 milioni di anni per una variet‡ di uranio a una piccola frazione di secondo per una variet‡ di polonio.
Il radon Ë a sua volta radioattivo e si trasforma in un altro elemento, il polonio. Successivi cambiamenti portano al piombo (7O" Pb), che Ë stabile, cioË non si scompone ulteriormente. Altre serie di elementi radioattivi hanno inizio con l'uranio, il torio e l'attinio e finiscono come isotopi del piombo.
|
Torna alla Home Base
|
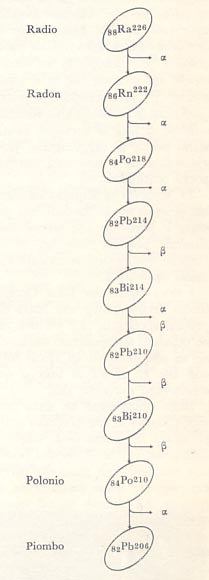
A destra: stadi successivi nella divisione di un atomo di radio: l'atomo emette una particella alfa e si trasforma in radon che poi si muta in polonio.L'ultimo stadio Ë il piombo che non muta. I numeri a destra dei simboli indicano il peso atomico mentre quelli a sinistra il numero atomico nei diversi stadi.
|
|
|
|