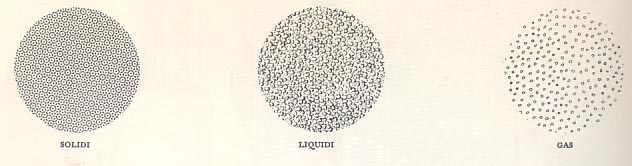
Dalla foto sopra si nota che la materia si presenta in tre stati: solido, liquido e gassoso.
In genere si pensa ai metalli come a dei solidi, ma il mercurio, che č un comune metallo, a temperatura ambiente č liquido. Inoltre, a grandi profonditą nell'interno della Terra, le rocce si comportano come liquidi a causa della grande pressione esistente nell'intemo della massa terrestre. Sebbene sia un gas, l'anidride carbonica puņ esser compressa in un blocco solido chiamato "ghiaccio secco"; tuttavia, se lasciamo questo blocco in una stanza calda, esso si trasforma di nuovo spontaneamente in gas.
Finché gli scienziati non ebbero appreso sufficienti notizie sugli atomi e sulle molecole, fu difficile per l'uomo spiegarsi in che modo questi tre stati della materia (lo stato gassoso, lo stato liquido e quello solido) differiscano l'uno dall'altro.
Tutte le sostanze, diventano solide quando viene sottratta loro una quantitą sufficiente di calore. L'unica eccezione č costituita dall'elio, perché questo gas si solidifica solo quando č sottoposto a una pressione considerevole. In un solido le molecole sono raggruppate cosķ strettamente che, in genere, si dispongono secondo uno schema regolare, ciņ che noi chiamiamo un cristallo. Ciascuna molecola e tenuta al suo posto dall'attrazione delle sue vicine, ed č necessaria una grande forza per separarle.
Nel disegno di un cristallo di sale comune, lo schema č cosķ regolare che non possiamo distinguere le molecole originali riunitesi al momento della cristallizzazione.
Sebbene fortemente tenute assieme, le molecole dei solidi sono in costante movimento, senza tuttavia perdere ognuna il proprio posto nello schema. Inoltre ciascun atomo in un solido possiede una notevole libertą di movimento, dato che puņ cambiare la propria energia vibratoria e il proprio senso di rotazione non solo nella direzione, ma anche nella quantitą. L'energia totale di ciascun atomo č uguale alla quantitą di calore che esso fornisce al solido.
Quando l'energia di alcuni atomi di un solido viene accresciuta riscaldando il solido alla fiamma, essi trasmettono la propria energia agli atomi vicini finché
tutti gli atomi hanno piś o meno la stessa quantitą di energia. Via via che l'energia aumenta gli atomi si muovono tanto rapidamente che le forze di attrazione fra molecole adiacenti non sono pił forti a sufficienza per tenerle unite; alcune molecole e gruppi di molecole si staccano dalla superficie del solido e scivolano su di essa, unendosi ad altre molecole per separarsene subito di nuovo. Quando tutte le molecole hanno acquistato questa accresciuta libertą, l'aspetto della sostanza č completamente diverso; infatti essa č ora un liquido che puņ essere diviso, mutato nella forma e versato molto facilmente. Ma le molecole, sebbene scorrano l'una sull'altra, sono ancora fortemente attratte. Osserviamo il comportamento di una goccia di mercurio su un piatto o di una goccia d'acqua su un blocco di cera: č evidente che le molecole della goccia "preferiscono" stare tutte raggruppate.
Se aggiungiamo altra energia al liquido, le sue molecole perdono la tendenza a restare unite ed abbiamo cosģ un gas, le cui molecole si muovono liberamente in tutte le direzioni. Esse hanno bisogno di essere contenute da tutti i lati ed occupano interamente qualsiasi luogo chiuso.
Conosciamo meglio il comportamento delle molecole nei gas che nei liquidi o nei solidi. La velocitą media delle molecole dell'aria, ad esempio, č piś di 1600 chilometri all'ora ed esse "urtano" le une contro le altre continuamente, movendosi solo di centesimi di micron fra un urto e l'altro.
Torna alla Home Base
|

Sopra: fabbricazione di pallini da sparo: il piombo fuso viene fatto cadere da una certa altezza attraverso un setaccio; poi, come tutti i liquidi il piombo fuso tende ad assumere una forma sferica.
Sotto: una bolla di sapone presenta una forma sferica cioč la forma pił compatta possibile; la sua superficie č sottoposta a una tensione superficiale.
|